 واضح آرشیو وب فارسی:خبر آنلاین:
واضح آرشیو وب فارسی:خبر آنلاین:
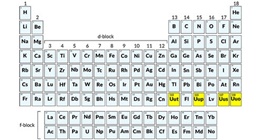
ردیف هفتم جدول مندلیف چطور با جای ثابت 4 عنصر کامل شد؟/همه چیز درباره اتفاق مهم شیمی دانش > دانشهای بنیادی - 4 عنصر در جدول تناوبی عناصر سرانجام جای و خانه ثابت خودشان را پیدا کردند تا دوره هفتم این جدول مشهور که به نام مندلیف مشهور است هم پر شود. آیا نوبت به ردیفهای جدید میرسد؟
در حالي كه كشورهاي مختلف درگير جشنهاي سال نو ميلادي بودند اتحادیه بینالمللی شیمی محض و کاربردی موسوم به آيوپاك خبر مهمي را اعلام كرد. به صورت رسمي 4 عنصر توانستند خانه و جايگاه خود را در دوره 7 جدول تناوبي به دست آورند. تمام عنصرهای با عدد اتمی ۹۹ تا ۱۱۲ (که مابین اینشتینیم و کوپرنیسیم قرار دارند) و نیز دو عنصر فلروویوم و لیورموریوم، در طبیعت پدید نیامدهاند، بلکه در آزمایشگاه ساخته شدهاند. سپس آیوپاک آنها را به طور رسمی پذیرفتهاست. اما عناصر خانههاي ۱۱۳، ۱۱۵، ۱۱۷ و ۱۱۸ هر چند در آزمايشگاه ساخته شده بودند اما تا پيش از اين مورد تائيد اتحادیه بینالمللی شیمی محض و کاربردی قرار نگرفته بودند. اما حالا آيوپاك اعلام كرده كه یک تیم مشترک آمریکایی (آزمایشگاه ملی لاورنس لیوِر مور واقع در کالیفرنیا) و روسی (انستیتوی مشترک تحقیقات هسته ای واقع در دوبنا) عناصر ۱۱۵، ۱۱۷ و ۱۱۸ را ساختهاند و به تائيد اين نهاد رساندهاند. همچنين عنصر ۱۱۳ هم توسط دانشمندان ژاپنی (موسسه تجامع تحقیقاتی ریکِن) ساخته شده و مورد تائيد آيوپاك قرار گرفته است.
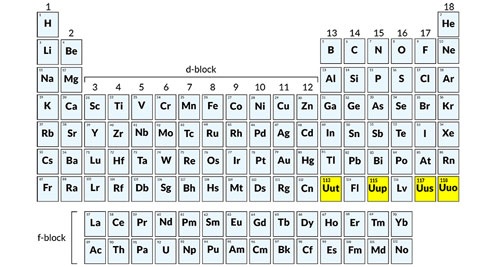
تا پيش از اين ، جدول تناوبی ۱۱۸ عنصر داشت که ۱۱۴ عنصر به صورت رسمی از سوی اتحادیه بینالمللی شیمی محض و کاربردی پذیرفته و نامگذاری شده بودند اما 4 عنصر ديگر مورد تائيد رسمي قرار نگرفته بودند. با اين موفقيت حالا رديف هفتم اين جدول هم با اين 4 عنصر به صورت رسمي كامل شده است. ۹۸ عنصر از مجموع ۱۱۸ عنصر در طبیعت یافت میشوند و از آن میان، ۸۴ مورد، عناصر پایدار یا دارای نیمعمر بیش از سن زمین هستند. در حالی که ۱۴ عنصر باقیمانده نیمعمر کوتاهی دارند یا به عبارت دیگر پرتوزا هستند. در حال حاضر، این عناصر تنها بر اثر انجام واکنش هستهای در عناصر دیگر به وجود میآیند و فراوانی ناچیزی دارند.
جدول تناوبی در سال 1869 توسط ديميتری ايوانوويچ مندليف شيميدان و مخترع روس معرفی شد. در جدول تناوبی يا مندليف عناصر شيميايی بر اساس عدد اتمی خود در رديفها و ستونهای جدول قرار میگيرند. عدد اتمی عبارت است از تعداد پروتونهاي موجود در هسته اتم. اولين عنصر جدول تناوبی هيدروژن با عدد اتمی 1 است که در هسته اتم آن يک پروتون وجود دارد. آخرین عنصر جدول تناوبی نيز عنصر تازه کشف شده 118 با نام موقت Ununoctium است که 118 پروتون در هسته آن قرار گرفته است.
از چهار عنصری که کشف آنها توسط اتحاديه بينالمللی شيمی محض و کاربردی تايید شده نيمه عمر Uut يا اونونتریوم حدود 20 ثانيه، Uup يا اونونپنتیوم حدود 220 ميلی ثانيه، Uus يا اونونسپتیوم حدود 330 روز، و نيمه عمر Uuo يا اونونوکتیوم حدود 89 صدم ثانيه است. نيمه عمر يک عنصر عبارت است از مدت زمان مورد نياز برای از بين رفتن نيمی از ايزوتوپ راديواکتيو آن عنصر. هنوز روشن نیست که آیا عنصرهای تازهتر که در آینده شناسایی میشوند در ردیف هشتم (دورهٔ هشتم) جای میگیرند یا به کلی نظم جدول را به هم میریزند. گلن سیبورگ بر این باور بود که دورهٔ هشتم جدول به گونهای است که دو عنصر ۱۱۹ و ۱۲۰ از بلوک اس، ۱۸ عنصر از بلوک جدید جی و ۳۰ عنصر از بلوکهای اف، دی و پی را دربر میگیرد. برخی فیزیکدانان معاصر مانند پکا پیکو به صورت نظری به این نتیجه رسیدهاند که این عنصرهای تازهتر، از اصل آفبا که توضیحدهندهٔ چگونگی پُر شدن لایههای الکترونی است، پیروی نخواهند کرد. به این ترتیب با شناسایی عنصرهای تازهتر، ظاهر جدول تناوبی دچار دگرگونی خواهد شد. 5454
کلید واژه ها: شیمی -
شنبه 12 دی 1394 - 19:54:32
این صفحه را در گوگل محبوب کنید
[ارسال شده از: خبر آنلاین]
[تعداد بازديد از اين مطلب: 174]
















